Đốt cháy 21 gam chất X là dẫn xuất benzen (CTPT trùng với CTĐGN), thu được 23,52 lit CO2 (đktc) và 10,8 gam H2O. Mặt khác, 21 gam X tác dụng vừa đủ với dung dịch NaOH thu được 27,6...
Câu hỏi :
Đốt cháy 21 gam chất X là dẫn xuất benzen (CTPT trùng với CTĐGN), thu được 23,52 lit CO2 (đktc) và 10,8 gam H2O. Mặt khác, 21 gam X tác dụng vừa đủ với dung dịch NaOH thu được 27,6 gam muối. Số CTCT của X là:
A.7
B.5
C.6
D. 12
* Đáp án
* Hướng dẫn giải
Trả lời:
Vì đốt cháy X thu được CO2 và H2O → trong X chứa C, H và có thể có O
\[{n_{C{O_2}}} = \frac{{23,52}}{{22,4}} = 1,05\left( {mol} \right)\]
\[{n_{{H_2}O}} = \frac{{10,8}}{{18}} = 0,6\left( {mol} \right)\]
Áp dụng định luật bảo toàn khối lượng:
\[{m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}}\]
→ \[{m_{C{O_2}}}\] = 1,05.44 + 0,6.18 – 21 = 36 gam
→ \[{n_{{O_2}}}\] = 1,125 mol
Nhận thấy:
\[2.{n_{{O_2}}}
→ trong X chứa O
Áp dụng định luật bảo toàn nguyên tử:
\[{n_{O\,trong\,}}_X = 2.{n_{C{O_2}}} + {n_{{H_2}O}} - 2.{n_{{O_2}}} = 2.1,05 + 0,6 - 2.1,125 = 0,45\,mol\]
\[{n_{C\,trong\,}}_X = {n_{C{O_2}}} = 1,05\,mol\]\[{n_{H\,trong\,}}_X = 2.{n_{{H_2}O}} = 1,2\,mol\]
\[ \to {n_C}_X:{n_H}:{n_O} = 1,05:1,2:0,45\, = 7:8:3\]
→ CTĐGN của X là C7H8O3
Vì CTPT của X trùng với CTĐGN
→ CTPT của X là C7H8O3
\[{n_{{C_7}{H_8}{O_3}}} = \frac{{21}}{{140}} = 0,15mol\]
X tác dụng với dung dịch NaOH:
Cứ thay thế 1 nguyên tử H bằng 1 nguyên tử Na thì khối lượng tăng:
23 – 1 = 22
Mà theo bài, khối lượng tăng 27,6 – 21 = 6,6 gam
+)số mol NaOH phản ứng là:
\[{n_{NaOH}} = \frac{{6,6}}{{22}} = 0,3mol\]
\[ \to {n_{{C_7}{H_8}{O_3}}} = 2{n_{NaOH}}\]
→ trong X có 2 nhóm -OH tác dụng với NaOH
→ X có 2 nhóm -OH phenol và 1 nhóm -OH ancol hoặc X có 2 nhóm -OH phenol và 1 nhóm ete
Các CTCT của X là
TH1
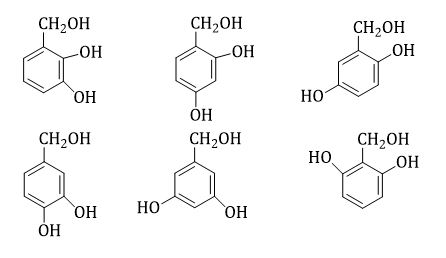
TH2: Thay -CH2OH bằng -OCH3 (6 công thức)
Đáp án cần chọn là: D
>Câu hỏi trên thuộc đề trắc nghiệm dưới đây !
Phenol !!
Copyright © 2021 HOCTAP247
