vi dụ Vd I: Nhúng một lá sắt nặng 10 g vào một dd CUSO4 Sau một thời gian lấy lá sắt ra cân lại thấy nặng10,4 g Hoi có bao nhi Vd 2: Cho 2,24 g bột Fe vào
Lời giải 1 :
Bạn xem hình

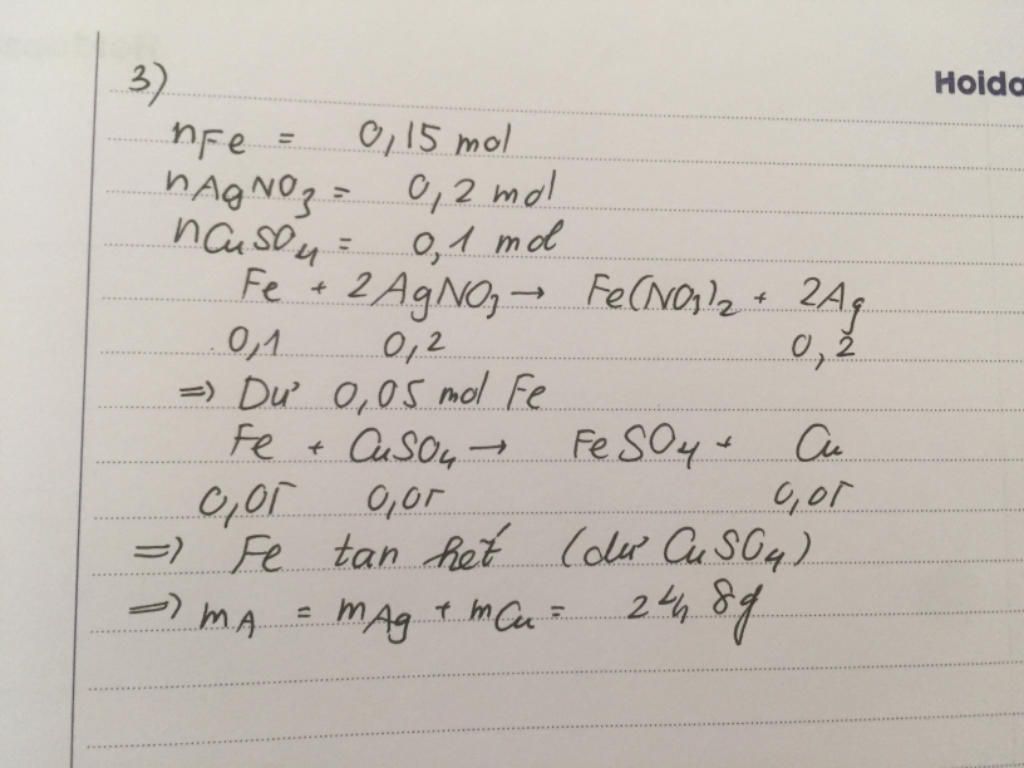
Thảo luận
Lời giải 2 :
Đáp án:
Giải thích các bước giải:
Câu 1:
Khối lượng của dung dịch CuSO4= 25. 1,12 = 28 gam
m(CuSO4 )= (28. 15):100 = 4,2 gam ;n(CuSO4 )= 0,02625 mol
a) Phương trình hóa học:
Fe + CuSO4 → FeSO4 + Cu
56x gam 64x gam
b) Cứ 1 mol Fe phản ứng tạo thành 1 mol Cu thì khối lượng thanh Fe tăng 64 - 56 = 8 gam
Có x mol Fe phản ứng tăng 2,58 - 2,5 = 0,08 gam
\( \to x = 0,08 : 8 =0,01 mol\)
Dung dịch sau phản ứng chứa FeSO4 0,01 mol hay 1,52 gam và CuSO4 dư 0,02625 - 0,01 = 0,01625 mol hay 2,6 gam
Khối lượng dung dịch sau phản ứng: mdd = \( m_{dd CuSO_{4}}\) + mFe(p.ư) – mCu = 25.1,12 + 0,01.56 - 0,01.64 = 27,91 g
Nồng độ C% chất tan:
C% CuSO4 = \( \dfrac{0,01625.160}{27,91}\).100% ≈ 9,32%
C% FeSO4 = \( \dfrac{0,01.152}{27,91}\).100% ≈ 5,45%
Câu 2:
`Zn + Pb(NO_3)_2 → Zn(NO_3)_2 + Pb↓`
` x 0,02 0,02 x `
`n_{Pb(NO_3)_2}=0,5.2=1\ mol`
Gọi x là số mol của Pb
Ta có : `207x - 65 x = 2,84`
`142x = 2,84 `
`x = 0,02 `
a. `m_{Pb}=207.0,02=4,14\ gam`
b. `n_{Pb(NO_3)_2\ tham\ gia}=0,02\ mol`
`n_{Pb{NO_3}_2\ dư}=1-0,02=0,98\ mol`
`CM_{Pb(NO_3)_2}=\frac{0,98}{0,5}=1,96M`
`n_{ZnSO_4}=0,02\ mol`
`CM_{ZnSO_4}=\frac{0,02}{0,5}=0,04M`
Có thể bạn quan tâm
Bạn có biết?
Hóa học, một nhánh của khoa học tự nhiên, là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất.Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó.Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học.
Nguồn : Wikipedia - Bách khoa toàn thưTâm sự 9
Lớp 9 - Là năm cuối ở cấp trung học cơ sở, sắp phải bước vào một kì thi căng thẳng và sắp chia tay bạn bè, thầy cô và cả kì vọng của phụ huynh ngày càng lớn mang tên "Lên cấp 3". Thật là áp lực nhưng các em hãy cứ tự tin vào bản thân là sẻ vượt qua nhé!
Nguồn : ADMIN :))Copyright © 2021 HOCTAP247

