Cho nhôm phản ứng với axit clohiddric thu được muối clorua và nhôm cloura (alcl3) và 3,36 (khí hidrô ở đktc) A. Tính khối lượng nhôm cần dùng B. Tính khối lư
Cho nhôm phản ứng với axit clohiddric thu được muối clorua và nhôm cloura (alcl3) và 3,36 (khí hidrô ở đktc) A. Tính khối lượng nhôm cần dùng B. Tính khối lượng muối alcl3 thu đc C. Đặt thêm đề
Lời giải 1 :
Đáp án:
Giải thích các bước giải:
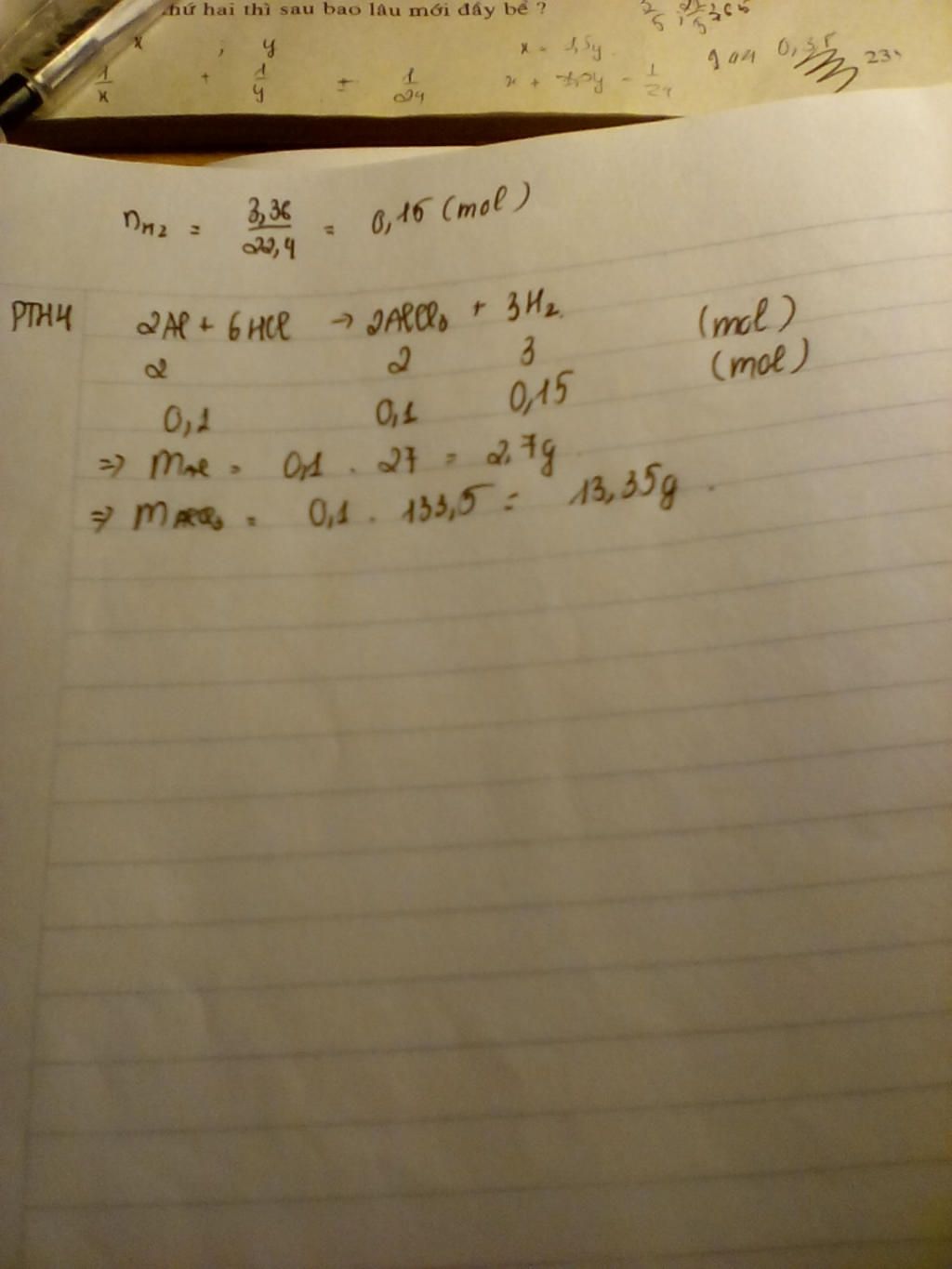
Thảo luận
Lời giải 2 :
Đáp án:
Giải thích các bước giải:
Đặt thêm đề là sao? Tự đặt đề á.
c, Tính khối lượng $HCl$ cần dùng
$PTHH:2Al+6HCl\to 2AlCl_3+3H_2$
$n_{H_2}=\dfrac{3.36}{22.4}=0.15(mol)$
$Theopt:n_{Al}=n_{AlCl_3}=\dfrac{2}{3}n_{H_2}=0.1(mol)$
$m_{Al}=0.1\times27=2.7(g)$
$m_{AlCl_3}=0.1\times133.5=13.35(g)$
$Theopt:n_{HCl}=2n_{H_2}=0.3(mol)$
$m_{HCl}=0.3\times36.5=10.95(g)$
Có thể bạn quan tâm
Bạn có biết?
Hóa học, một nhánh của khoa học tự nhiên, là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất.Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó.Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học.
Nguồn : Wikipedia - Bách khoa toàn thưTâm sự 8
Lớp 8 - Năm thứ ba ở cấp trung học cơ sở, học tập bắt đầu nặng dần, sang năm lại là năm cuối cấp áp lực lớn dần nhưng các em vẫn phải chú ý sức khỏe nhé!
Nguồn : ADMIN :))Copyright © 2021 HOCTAP247
