Đốt cháy 16,8 gam sắt trong bình chứa 6,72 lit oxi (đktc) thu được oxit sắt từ. a) Chất nào còn dư sau phản ứng? Dư bao nhiêu mol? b) Tính khối lượng sản phẩm
Đốt cháy 16,8 gam sắt trong bình chứa 6,72 lit oxi (đktc) thu được oxit sắt từ. a) Chất nào còn dư sau phản ứng? Dư bao nhiêu mol? b) Tính khối lượng sản phẩm thu được?
Lời giải 1 :
Bạn tham khảo nha!
$3Fe$ + $2O_{2}$ -> $Fe_{3}$$O_{4}$
a. $n_{Fe}$= $\dfrac{16,8}{56}$= $0,3$ mol
$n_{O2}$= $\dfrac{6,72}{22,4}$= $0,3$ mol
Theo tỉ lệ mol 2 chất, ta có:
$\dfrac{0,3}{3}$ < $\dfrac{0,3}{2}$
=> $O_{2}$ dư
=> $n_{O2 dư}$= $(0,15 - 0,1)$ =$0,05$ mol
b. $m_{Fe3O4}$= $0,1× (56× 3+ 16× 4)$= $23,2$ $g$
Thảo luận
Lời giải 2 :
Đáp án:
Giải thích các bước giải:
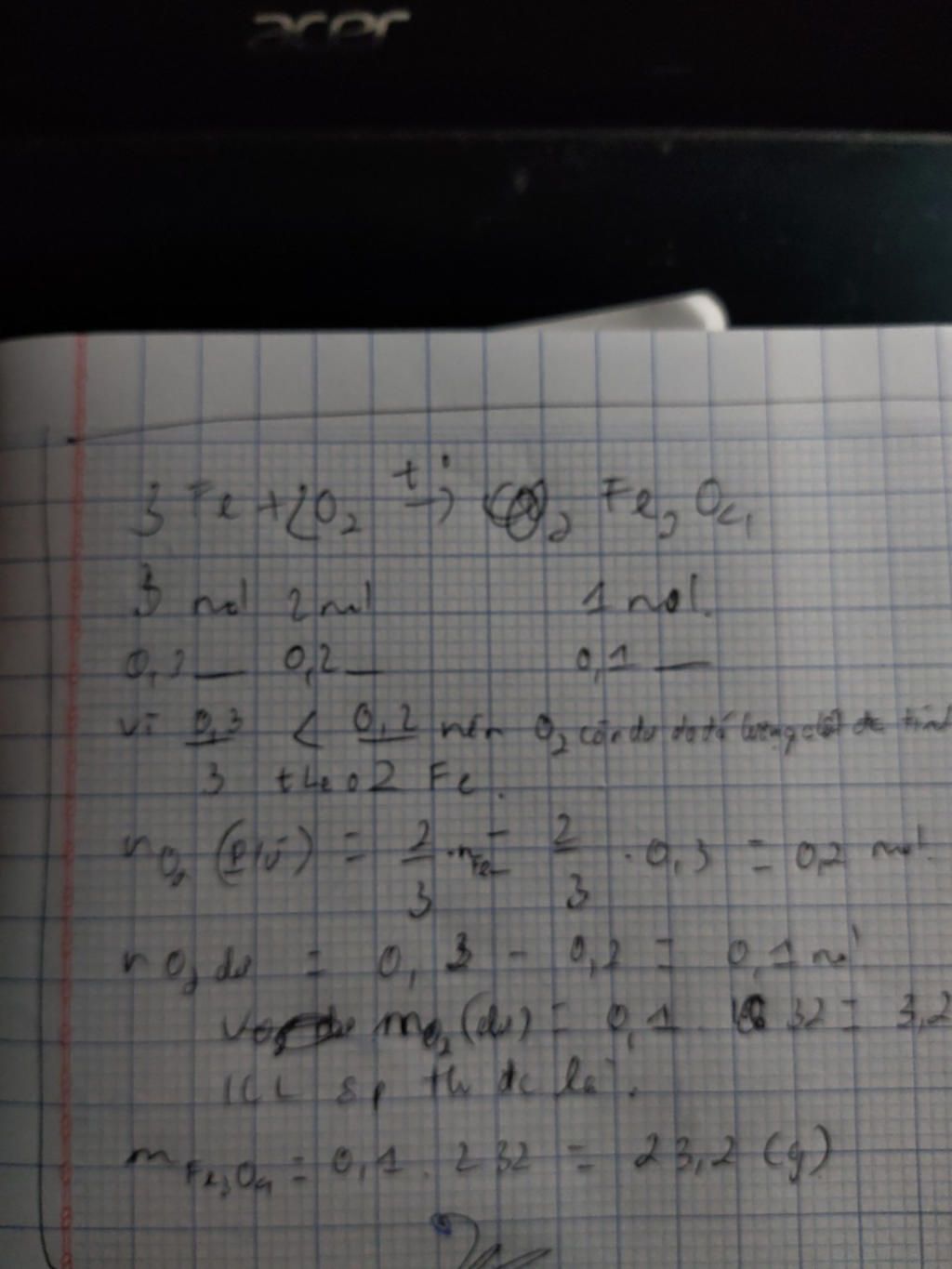
Có thể bạn quan tâm
Bạn có biết?
Hóa học, một nhánh của khoa học tự nhiên, là ngành nghiên cứu về thành phần, cấu trúc, tính chất, và sự thay đổi của vật chất.Hóa học nói về các nguyên tố, hợp chất, nguyên tử, phân tử, và các phản ứng hóa học xảy ra giữa những thành phần đó.Hóa học đôi khi được gọi là "khoa học trung tâm" vì nó là cầu nối các ngành khoa học tự nhiên khác như vật lý học, địa chất học và sinh học.
Nguồn : Wikipedia - Bách khoa toàn thưTâm sự 8
Lớp 8 - Năm thứ ba ở cấp trung học cơ sở, học tập bắt đầu nặng dần, sang năm lại là năm cuối cấp áp lực lớn dần nhưng các em vẫn phải chú ý sức khỏe nhé!
Nguồn : ADMIN :))Copyright © 2021 HOCTAP247
