Hoá học 11 Bài 35: Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
Tóm tắt bài
1.1. BENZEN VÀ ĐỒNG ĐẲNG
1.1.1. Đồng đẳng, đồng phân, danh pháp, cấu tạo
Dãy đồng đẳng của benzen
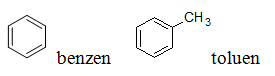
- C6H6 (benzen), C7H8 (toluen), C8H10, ... , CnH2n-6 (n ≥ 6, nguyên)
Đồng phân, danh pháp
Đồng phân
- C6H6 và C7H8 không có đồng phân hidrocacbon thơm.
- Từ C8H10 trở đi có:
- đồng phân vị trí tương đối của các nhóm ankyl
- đồng phân cấu tạo mạch cacbon của nhánh
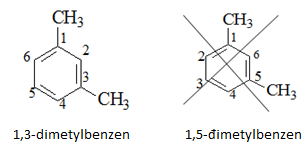
- Ví dụ: Đồng phân của C8H10
.PNG)
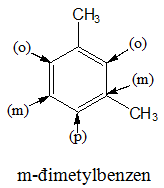
Đồng phân vị trí tương đối của các nhóm ankyl
a) o-xilen; b) m-xilen; c) p-xilen
- Đối với nhóm thế có từ 3C trở lên thì các em có thêm đồng phân cấu tạo mạch C của nhánh.
Danh pháp
- Tên hệ thống: nhóm ankyl + benzen
- Chú ý: Nếu vòng benzen liên kết với nhiều nhóm ankyl tên gọi: số chỉ vị trí nhánh + tên nhánh + benzen
- Cách đánh số các nguyên tử C trong vòng benzen sao cho tổng chỉ số trong tên gọi là nhỏ nhất.
Cấu tạo
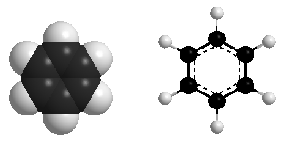
Hình 1: Mô hình benzen
- Có 3 liên kết đôi, có cấu trúc lục giác đều.
- Cả 6 nguyên tử C và 6 nguyên tử H cùng nằm trên một mặt phẳng.
- Có hai cách biểu diễn công thức của benzen:
1.1.2. Tính chất vật lí
- Các hiđrocacbon thơm đều là chất lỏng hoặc rắn ở điều kiện thường ; ts, tnc tăng theo chiều tăng của phân tử khối.
- Hiđrocacbon thơm ở thể lỏng có mùi đặc trưng, không tan trong nước, nhẹ hơn nước, hòa tan được nhiều chất hữu cơ.
1.1.3. Tính chất hóa học
Benzen tương đối dễ tham gia phản ứng thế hơn so với các chất oxi hóa. Đó cũng chính là tính chất hóa học đặc trưng chung của các hiđrocacbon thơm nên được gọi là tính thơm
Thế nguyên tử H của vòng benzen
a) Phản ứng với halogen
- Benzen phản ứng thế với brom:
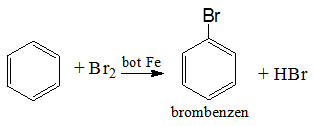
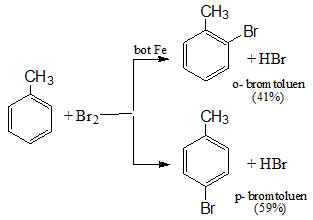
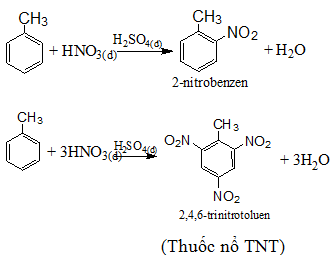
- Toluen tác dụng với brom:
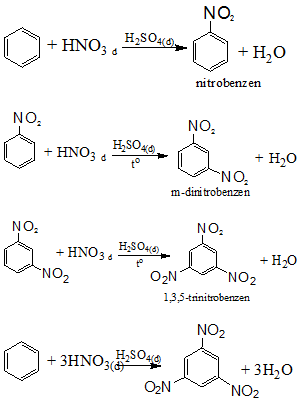
- Phản ứng với axit nitric:
- Quy tắc thế ở vòng benzen: khi ở vòng benzen đã có sẵn nhóm ankyl (hay các nhóm –OH, -NH2, -OCH3,...), phản ứng thế vào vòng sẽ dễ dàng hơn và ưu tiên thế vào vị trí o-, p-. Nếu vòng benzen đã có sẵn nhóm –NO2 ( hoặc các nhóm –COOH, -SO3H, ...) phản ứng thế vào vòng sẽ khó hơn và ưu tiên xảy ra ở vị trí m-.
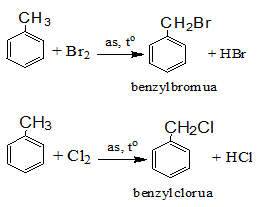
b) Thế nguyên tử H của mạch nhánh
Phản ứng cộng
a) Cộng Hidro
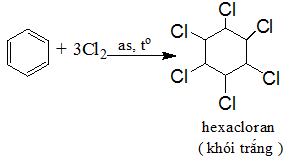
b) Cộng Clo
- Chú ý: Phản ứng này được dùng để sản xuất thuốc trừ sâu 666 nhưng do chất này có độc tính cao và phân hủy chậm nên ngày nay không được sử dụng.
Phản ứng oxi hóa
a) Phản ứng oxi hóa không hoàn toàn
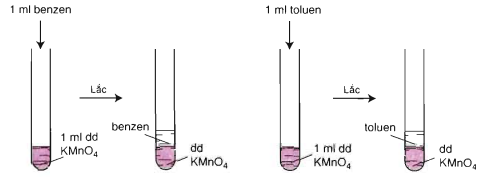
Hình 2: Benzen và toluen không làm mất màu dung dịch KMnO4 ở điều kiện thường
Khi đun nóng hai ống nghiệm trong nồi cách thủy:
- Benzen vẫn không làm mất màu dung dịch KMnO4
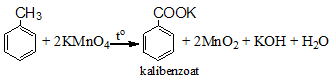
- Toluen làm mất màu dung dịch KMnO4 , tạo kết tủa MnO2
b) Phản ứng oxi hóa hoàn toàn
Nhận xét: Số mol CO2 luôn lớn hơn số mol H2O
1.2. MỘT SỐ HIDROCACBON THƠM KHÁC
1.2.1. STIREN
Cấu tạo và tính chất vật lí
a) Cấu tạo
- Stiren có CTPT: C8H8
- Công thức cấu tạo:
b) Tính chất vật lí
Stiren (còn gọi là Vinylbenzen) là chất lỏng, không màu, sôi ở 146oC, không tan trong nước nhưng tan nhiều trong dung môi hữu cơ.
Tính chất hóa học
Stiren có đặc điểm phần nhánh giống etilen, phần vòng giống benzen. Vì vậy, stiren thể hiện tính chất hóa học giống etilen ở phần mạch nhánh và thể hiện tính chất giống benzen ở phần nhân thơm.
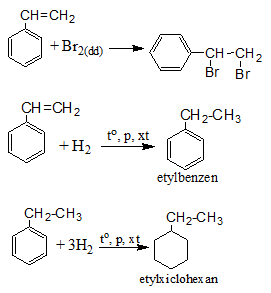
a) Phản ứng cộng
b) Phản ứng trùng hợp
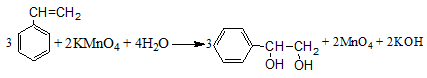
c) Phản ứng oxi hóa
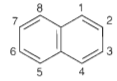
1.2.2. NAPHTALEN
Cấu tạo và tính chất vật lí
- Công thức phân tử: C10H8
- Công thức cấu tạo:
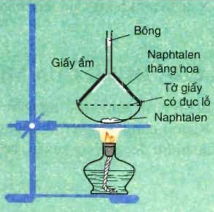
- Naphtalen (băng phiến) là chất rắn, nóng chảy ở 80oC, tan trong benzen, ete, ... và có tính thăng hoa.
Hình 3: Thí nghiệm Naphtalen thăng hoa
Tính chất hóa học
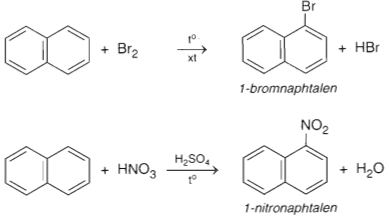
a) Phản ứng thế
b) Phản ứng cộng
1.3. MỘT SỐ ỨNG DỤNG CỦA HIDROCACBON THƠM
Hình 4: Ứng dụng của hidrocacbon
Bài 1:
Nhận biết các chất lỏng riêng biệt: ancol etylic, clorofom, benzen bằng 1 thuốc thử nào sau đây?
Hướng dẫn:
Dùng H2O ⇒ benzen phân lớp còn 2 chất còn lại tan.
Sau đó cho 2 chất còn lại vào benzen. Vì benzen tan rất kém trong nước và rượu nên sẽ phân lớp nếu có ancol etylic và tan tốt trong dung môi hữu cơ là clorofom.
Bài 2:
Cho sơ đồ phản ứng sau: \(Toluen \xrightarrow[1:1]{+Cl_2\ (as)} X \xrightarrow[]{+NaOH,t^0} Y \xrightarrow[]{+CuO,t^0} Z \xrightarrow[]{dd\ AgNO_3/NH_3} T\)
Biết rằng X, Y, Z, T là những sản phẩm chính. Công thức cấu tạo của chất T là:
Hướng dẫn:
\(\\C_6H_5CH_3 \xrightarrow[1:1]{+Cl_2,as} C_6H_5CH_2Cl \xrightarrow[]{+NaOH,t^0} C_6H_5CH_2OH\\ C_6H_5CH_2OH \xrightarrow[]{+CuO,t^0} C_6H_5CHO \xrightarrow[]{dd.AgNO_3/NH_3} C_6H_5COONH_4\)
Bài 3:
Cho 17,08 gam hỗn hợp X gồm hai hợp chất hữu cơ đơn chức là dẫn xuất của benzen và có cùng công thức phân tử C7H6O2 tác dụng với lượng dư dung dịch AgNO3 trong NH3 (đun nóng), thu được 10,8 gam Ag. Cho 8,54 gam X nói trên tác dụng với 100 ml dung dịch NaOH 1,0 M rồi cô cạn dung dịch sau phản ứng, thu được m gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Hướng dẫn:
X gồm : HCOOC6H5 và C6H5COOH
=> nHCOOC6H5 = ½ nAg = 0,05 mol
=> nC6H5COOH = 0,09 mol
8,54g X + NaOH (0,1 mol)
HCOOC6H5 + 2NaOH → HCOONa + C6H5ONa + H2O
C6H5COOH + NaOH → C6H5COONa + H2O
Chất rắn gồm : 0,025 mol HCOONa ; 0,025 mol C6H5ONa ; 0,045 mol C6H5COONa ; 0,005 mol NaOH
=> m = 11,28g
3. Luyện tập Bài 35 Hóa học 11
Sau bài học cần nắm:
- Định nghĩa, công thức chung, đặc điểm cấu tạo, đồng phân, danh pháp. Tính chất vật lí của benzen và đồng đẳng.
- Viết được công thức cấu tạo của benzen và một số chất trong dãy đồng đẳng. Viết được các phương trình hoá học biểu diễn tính chất hoá học của benzen, vận dụng quy tắc thế để dự đoán sản phẩm phản ứng. Xác định công thức phân tử, viết công thức cấu tạo và gọi tên.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 11 Bài 35 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. xuất hiện màu xanh.
- B. xuất hiện màu tím.
- C. có kết tủa màu trắng.
- D. có bọt khí thoát ra.
-
- A. Hai chất đó giống nhau về công thức phân tử và khác nhau về công thức đơn giản nhất
- B. Hai chất đó khác nhau về công thức phân tử và giống nhau về công thức đơn giản nhất
- C. Hai chất đó khác nhau về công thức phân tử và khác nhau về công thức đơn giản nhất
- D. Hai chất đó có cùng công thức phân tử và công thức đơn giản nhất
-
- A. Toluen.
- B. Stiren.
- C. Isopren.
- D. Etylbenzen.
-
- A. 74,25 gam.
- B. 49,5 gam.
- C. 45,9 gam.
- D. 24,75 gam.
-
- A. 12,5.
- B. 24.
- C. 16.
- D. 19,5.
-
- A. 4
- B. 2
- C. 3
- D. 5
Câu 3- Câu 5: Xem thêm phần trắc nghiệm để làm thử Online
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 11 Bài 35.
Bài tập 35.12 trang 55 SBT Hóa học 11
Bài tập 1 trang 191 SGK Hóa học 11 nâng cao
Bài tập 2 trang 191 SGK Hóa học 11 nâng cao
Bài tập 3 trang 191 SGK Hóa học 11 nâng cao
Bài tập 4 trang 192 SGK Hóa học 11 nâng cao
Bài tập 5 trang 192 SGK Hóa học 11 nâng cao
Bài tập 6 trang 192 SGK Hóa học 11 nâng cao
Bài tập 7 trang 192 SGK Hóa học 11 nâng cao
Bài tập 8 trang 192 SGK Hóa học 11 nâng cao
Bài tập 9 trang 192 SGK Hóa học 11 nâng cao
Bài tập 10 trang 192 SGK Hóa học 11 nâng cao
Bài tập 13 trang 160 Hóa học 11
4. Hỏi đáp về Bài 35 Chương 7 Hóa học 11
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
Copyright © 2021 HOCTAP247

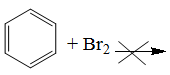
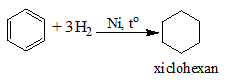
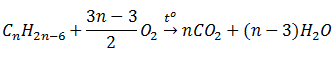
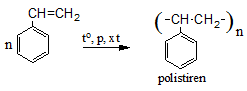
.PNG)
