Hoá học 9 Bài 41: Nhiên liệu
Tóm tắt bài
1.1. Nhiên liệu là gì?
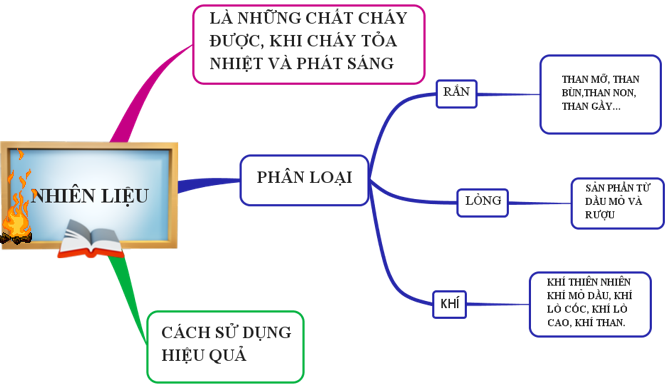
- Nhiên liệu là những chất cháy đựơc, khi cháy toả nhiệt và phát sáng.
- Lưu ý: Điện là một dạng năng lượng có thể phát sáng và toả nhiệt nhưng không phải là một loại nhiên liệu.
Hình 1: Nhiên liệu
1.2. Nhiên liệu đựơc phân loại như thế nào?
Căn cứ vào trạng thái sắp xếp các loại nhiên liệu làm 3 nhóm là rắn, lỏng, khí.
1.2.1. Nhiên liệu rắn
- Than:
- Than gầy: làm nhiên liệu.
- Than mỡ: Dùng để luyện than cốc.
- Than non: Dùng để làm nhiên liệu trong đời sống
- Than bùn: Làm chất đốt, phân bón tại chỗ.
- Gỗ
-
Than
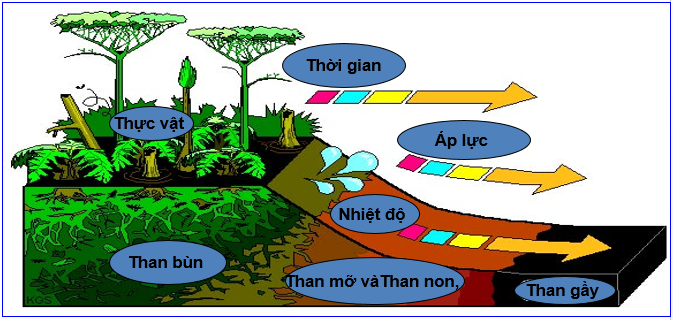
Hình 2: Quá trình hình thành than mỏ
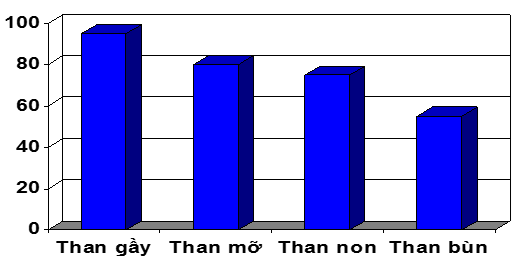
Hình 3: Hàm lượng Cacbon trong than
|
Than gầy |
Than mỡ |
Than non |
Than bùn |
|
|
Hàm lượng C |
90%C | 80%C | 78%C | 58%C |
|
Ứng dụng |
Dùng làm nhiên liệu trong công nghiệp. |
Dùng để luyện than cốc |
Dùng để luyện than cốc |
Dùng làm chất đốt tại chỗ và phân bón |
- Dưới lòng Đồng bằng sông Hồng, sâu đến 3500m là một bể than lớn, trữ lượng 210 tỷ tấn.
- Theo báo cáo than dưới lòng Đồng bằng sông Hồng nằm trên diện tích 3500km2, trải dài từ Hà Nội - Hưng Yên - Hải Dương - Thái Bình... rồi kéo thẳng ra biển. Có khoảng vài chục vỉa than với tổng trữ lượng dự báo là 210 tỷ tấn. Các vỉa than này có chiều dày lớn, dao động từ 2-3m đến 10-20m, ít lớp kẹp, vỉa nằm thoải, duy trì ổn định, chất lượng tốt...
- Theo số liệu khảo sát trên diện tích 962km2, thì trữ lượng than dự báo khoảng 30 tỷ tấn( khảo sát đến độ sâu 1700m). Trong đó tổng diện tích tìm kiếm tại huyện Khoái Châu (80km2) có trữ lượng than trên 1,5 tỷ tấn. Riêng khu vực Bình Minh (Khoái Châu) với diện tích thăm dò 25km2 đạt thăm dò sơ bộ trữ lượng 456 triệu tấn (khảo sát đến độ sâu 600m).
- Gỗ
Hình 4: Ứng dụng của gỗ
- Gỗ là loại nhiên liệu được sử dụng từ thời cổ xưa. Song việc sử dụng gỗ làm nhiên liệu lãng phí rất lớn nên ngày càng bị hạn chế. Hiện nay, gỗ chủ yếu được sử dụng làm vật liệu trong xây dựng và nguyên liệu cho công nghiệp
1.2.2. Nguyên liệu lỏng
- Gồm các sản phẩm chế biến từ dầu mỏ (xăng, dầu hỏa...) và rượu. Nhiên liệu lỏng được dùng chủ yếu cho các động cơ đốt trong, một phần nhỏ dùng để đun nấu và thắp sáng.
-
Xăng là hỗn hợp của các Hiđrocacbon no, mạch thẳng (CnH2n+2) chứa từ 7 – 11 nguyên tử C.
-
Dầu hỏa cũng là hỗn hợp của các Hiđrocacbon no, mạch thẳng (CnH2n+2) nhưng chứa từ 12 – 15 nguyên tử C.
-
Êtanol (Rượu Etylic hay Cồn) là một ancol mạch thẳng, công thức phân tử của nó là C2H6O. Công thức cấu tạo là C2H5OH hay CH3-CH2-OH
Hình 5: Cồn khô, cồn thạch, cồn lỏng
Hình 6: Ứng dụng của nhiên liệu lỏng
- Xăng sinh học E5 là nhiên liệu chứa 5% thể tích cồn sinh học và 95% thể tích xăng truyền thống. Bên cạnh đó, việc sử dụng nhiên liệu được cho là hành động thiết thực để bảo vệ môi trường. Vì NLSH là loại nhiên liệu được chế xuất từ các hợp chất có nguồn gốc động thực vật như trên nên nó là sản phẩm hoàn toàn thân thiện với môi trường và là nguồn nhiên liệu tái sinh được.
- Sử dụng nhiên liệu sinh học giúp giảm thiểu đáng kể các loại khí thải độc hại có trong các nhiên liệu truyền thống như CO, SO2, hạt bụi và khí. Ngoài ra, lượng khí độc hại CO2 thải ra môi trường của xăng sinh học ít hơn so với xăng truyền thống, làm giảm hiệu ứng nhà kính, giúp cho môi trường được an toàn và trong sạch hơn.
1.2.3. Nguyên liệu khí
- Gồm: Khí thiên nhiên, khí mỏ dầu, khí lò cốc, khí lò cao, khí than...
-
Năng suất tỏa nhiệt cao.
-
Dùng làm nhiên liệu.
-
Dễ cháy hoàn toàn, ít độc hại, không gây ô nhiễm
-
Hình 7: Năng suất tỏa nhiệt của một số nhiên liệu thông thường
1.3. Sử dụng nhiên liệu như thế nào cho hiệu quả?
- Cung cấp đủ oxi hoặc không khí cho sự cháy.
- Tăng diện tích tiếp xúc của nhiên liệu với không khí.
- Điều chỉnh lượng nhiên liệu để duy trì sự cháy ở mức độ cần thiết phù hợp với nhu cầu sử dụng.
1.4. Tổng kết
Hình 8: Sơ đồ tư duy bài Nhiên liệu
Bài 1:
Biết 1 mol cacbon khi cháy hoàn toàn tỏa ra một nhiệt lượng là 394kJ. Tính nhiệt lượng tỏa ra khi đốt cháy 5 kg than chứa 90% cacbon.
Hướng dẫn:
Khối lượng Cacbon là:
\({m_C} = 5 \times \frac{{90}}{{100}} = 4,5(kg)\)
Đổi 4,5 kg = 4,5.1000 gam
Số mol cacbon đem đi đốt là:
\({n_C} = \frac{{4,5}}{{12}} \times 1000 = 375(mol)\)
Nhiệt lượng tỏa ra là: 375 x 394 = 147750 (KJ)
3. Luyện tập Bài 41 Hóa học 9
Sau bài học cần nắm:
- Nhiên liệu là những chất cháy được, khi cháy toả nhiệt và phát sáng.
- Nắm đựơc cách phân loại nhiên liệu, đặc điểm và ứng dụng của một số loại nhiên liệu thông thường.
- Biết cách sử dụng nhiên liệu có hiệu quả, an toàn trong cuộc sống hàng ngày.
- Tính được nhiệt lượng toả ra khi đốt cháy than, khí metan và thể tích khí cacbonic tạo thành.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 9 Bài 41 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. Nguyên liệu.
- B. Nhiên liêu.
- C. vật liệu.
- D. Điện năng.
-
- A. Than mỡ.
- B. Than gầy.
- C. Than non.
- D. Than bùn.
-
- A. Cung cấp đủ oxi hoặc không khí cho sự cháy.
- B. Tăng diện tích tiếp xúc của nhiên liệu với không khí.
- C. Điều chỉnh lượng nhiên liệu để duy trì sự cháy ở mức độ cần thiết phù hợp với nhu cầu sử dụng.
- D. Cả ba ý trên đều đúng
Câu 3- Câu 5: Xem thêm phần trắc nghiệm để làm thử Online
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 9 Bài 41.
Bài tập 1 trang 132 SGK Hóa học 9
Bài tập 2 trang 132 SGK Hóa học 9
Bài tập 3 trang 132 SGK Hóa học 9
Bài tập 4 trang 132 SGK Hóa học 9
Bài tập 41.1 trang 51 SBT Hóa học 9
Bài tập 41.2 trang 51 SBT Hóa học 9
Bài tập 41.3 trang 51 SBT Hóa học 9
Bài tập 41.4 trang 51 SBT Hóa học 9
Bài tập 41.5 trang 51 SBT Hóa học 9
4. Hỏi đáp về Bài 41 chương 4 Hóa học 9
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
Copyright © 2021 HOCTAP247





.PNG)