Hoá học 8 Bài 27: Điều chế khí oxi - Phản ứng phân hủy
Tóm tắt bài
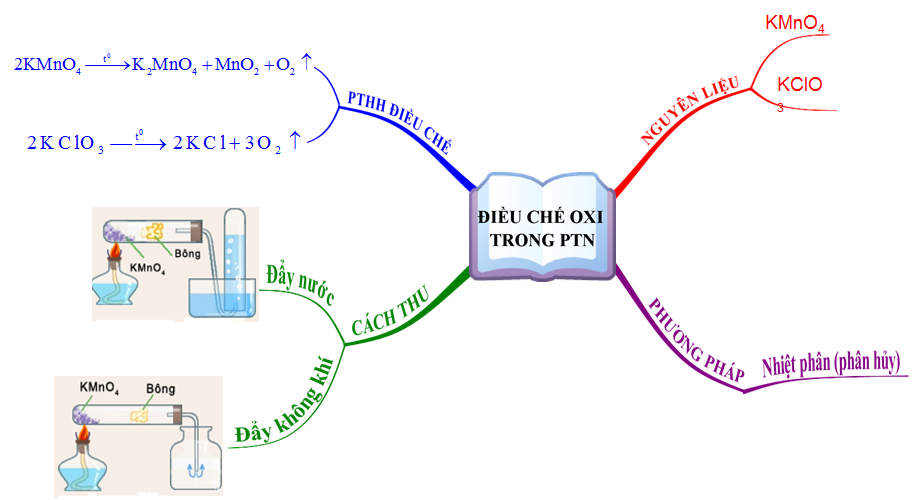
1.1. Điều chế khí oxi trong phòng thí nghiệm
Trong phòng thí nghiệm, khí oxi được điều chế bằng cách đun nóng những hợp chất giàu oxi và dễ bị phân hủy ở nhiệt độ cao như KMnO4 và KClO3.
1.1.1. Thí nghiệm
* Phản ứng nhiệt phân Kali pemanganat KMnO4
Video 1: Nhiệt phân Kali pemanganat KMnO4
- Khí oxi duy trì sự sống và sự cháy nên làm cho que đóm còn tàn than hồng bùng cháy.
- Phương trình hóa học: 2KMnO4
K2MnO4 + MnO2 + O2
* Phản ứng nhiệt phân Kali clorat
Video 2: Phản ứng nhiệt phân Kali clorat có xúc tác MnO2
- MnO2 đóng vai trò là chất xúc tác.
- Phương trình hóa học: 2 KClO3
2 KCl + 3 O2
1.1.2. Kết luận
- Kĩ năng tiến hành thí nghiệm:
-
Khi làm thí nghiệm phải hơ nóng đều ống nghiệm trước khi tập trung đun ở đáy ống nghiệm để ống nghiệm nóng đều à không bị vỡ.
-
Khi đun nóng KMnO4 ta phải đặt miếng bông ở đầu ống nghiệm để tránh thuốc tím theo ống dẫn khí thoát ra ngoài.
-
Vì khí oxi nặng hơn không khí nên khi thu khí oxi bằng cách đẩy không khí phải đặt miệng bình hướng lên trên và đầu ống dẫn khí phải để ở sát đáy bình.
-
Để biết được khí oxi trong bình đã đầy ta dùng que đóm đặt trên miệng ống nghiệm.
-
Khi thu oxi bằng cách đẩy nước ta phải chú ý: rút ống dẫn khí ra khỏi chậu trước khi tắt đèn cồn.
-
- Trong phòng thí nghiệm, khí oxi được điều chế bằng cách đun nóng những hợp chất giàu oxi và dễ bị phân hủy ở nhiệt độ cao như KMnO4 và KClO3.
- Có 2 cách thu khí oxi:
- Đẩy nước.
- Đẩy không khí.
Hình 1: Điều chế oxi trong phòng thí nghiệm
1.2. Sản xuất khí Oxi trong công nghiệp
- Trong thiên nhiên nguồn nguyên liệu được dùng để sản xuất khí oxi là nước và không khí.
- Các nguyên liệu để điều chế khí oxi trong phòng thí nghiệm không thể dùng để sản xuất khí oxi trong công nghiệp được vì các nguyên liệu này hiếm và mắc tiền.
- Lượng oxi được điều chế trong phòng thí nghiệm ít, quy mô sản xuất nhỏ và rất đắt.
- Không thể dùng thiết bị để điều chế khí oxi trong phòng thí nghiệm để điều chế khí oxi trong công nghiệp vì những thiết bị đó quá quá phức tạp.
1.2.1. Sản xuất khí oxi từ không khí
Bằng cách hạ không khí xuống dưới – 2000C, sau đó nâng dần dần nhiệt độ lên – 1830C ta thu được khí N2, hạ -1500C ta thu được khí oxi.
1.2.2. Sản xuất khí oxi từ nước
Người ta điện phân nước.
H2O điện phân → H2 + O2
1.3. Phản ứng phân hủy
| Phản ứng hóa học | Số chất phản ứng | Số chất sản phẩm |
2 KClO3 .PNG) 2 KCl + 3 O2 2 KCl + 3 O2 |
1 | 2 |
2KMnO4 .PNG) KMnO4 + MnO2 + O2 KMnO4 + MnO2 + O2 |
1 | 2 |
CaCO3 .PNG) CaO + CO2 CaO + CO2 |
1 | 2 |
⇒ Phản ứng phân hủy là phản ứng từ một chất ban đầu cho ra sản phẩm từ hai chất trở lên.
Phản ứng hóa hợp và phản ứng phân hủy trái ngược nhau.
Bài 1:
Thể tích khí Oxi sinh ra ở điều kiện tiêu chuẩn khi nhiệt phân 15,8 gam muối Kalipemanganat là?
Hướng dẫn:
Số mol KMnO4 là: \({n_{KMn{O_4}}} = \frac{{15,8}}{{158}} = 0,1(mol)\)
Phương trình hóa học:
2KMnO4 .PNG)
2 mol 1 mol
0,1 mol → 0,05 mol
Thể tích khí oxi sinh ra ở đktc là:
\({V_{{O_2}}} = 22,4.n = 22,4.0,05 = 1,12(lit)\)
Bài 2:
Nhiệt phân 12,25 gam muối Kaliclorat với xúc tác Mangan đioxit (MnO2) thấy thoát ra V lit khí không màu (đktc). Khí sinh ra là khí gì và có thể tích là bao nhiêu?
Hướng dẫn:
Số mol Muối Kaliclorat (KClO3) là:
\({n_{KCl{O_3}}} = \frac{m}{M} = \frac{{12,25}}{{122,5}} = 0,1(mol)\)
Phương trình hóa học:
2 KClO3 .PNG)
2 mol 3 mol
0,1 mol → 0,15 mol
Vậy theo phương trình thì khí không màu thoát ra là khí oxi
Thể tích khí oxi ở điều kiện tiêu chuẩn là:
\({V_{{O_2}}} = 22,4.n = 22,4.0,15 = 3,36(lit)\)
3. Luyện tập Bài 27 Hóa học 8
Sau bài học cần nắm:
- Phương pháp điều chế, thu khí oxi trong phòng thí nghiệm và trong công nghiệp.
- Phản ứng phân hủy là gì và lấy ví dụ minh họa.
- Khái niệm chất xúc tác, biết giải thích vì sao MnO2 được gọi là chất xúc tác trong phản ứng đun nóng hỗn hợp: KClO3 và MnO2.
3.1. Trắc nghiệm
Bài kiểm tra Trắc nghiệm Hóa học 8 Bài 27 có phương pháp và lời giải chi tiết giúp các em luyện tập và hiểu bài.
-
- A. b, c.
- B. b, d
- C. a,b,c.
- D. b, c, d
-
- A. khí oxi tan trong nước.
- B. khí oxi khó hóa lỏng.
- C. khí oxi ít tan trong nước.
- D. khí oxi nhẹ hơn nước.
-
- A. Que đóm tắt
- B. Que đóm bùng cháy
- C. Không có hiện tượng
- D. Que đóm cháy từ từ rồi tắt hẳn
-
- A. Đẩy nước và bình để đứng
- B. Đẩy không khí và bình để úp ngược
- C. Đẩy nước và bình để úp ngược
- D. ý B và C đều đúng
Câu 3- Câu 5: Xem thêm phần trắc nghiệm để làm thử Online
3.2. Bài tập SGK và Nâng cao
Các em có thể hệ thống lại nội dung bài học thông qua phần hướng dẫn Giải bài tập Hóa học 8 Bài 27.
Bài tập 4 trang 94 SGK Hóa học 8
Bài tập 5 trang 94 SGK Hóa học 8
Bài tập 6 trang 94 SGK Hóa học 8
Bài tập 27.1 trang 37 SBT Hóa học 8
Bài tập 27.2 trang 37 SBT Hóa học 8
Bài tập 27.3 trang 38 SBT Hóa học 8
Bài tập 27.4 trang 38 SBT Hóa học 8
Bài tập 27.5 trang 38 SBT Hóa học 8
Bài tập 27.6 trang 38 SBT Hóa học 8
Bài tập 27.7 trang 38 SBT Hóa học 8
Bài tập 27.8 trang 38 SBT Hóa học 8
Bài tập 27.9 trang 39 SBT Hóa học 8
4. Hỏi đáp về Bài 27 Chương 4 Hóa học 8
Trong quá trình học tập nếu có bất kì thắc mắc gì, các em hãy để lại lời nhắn ở mục Hỏi đáp để cùng cộng đồng Hóa HOC247 thảo luận và trả lời nhé.
Copyright © 2021 HOCTAP247