Trang chủ
Đề thi & kiểm tra
Lớp 9
Hóa học
Đề thi chính thức vào 10 môn Hóa Hệ chuyên THPT Chuyên Trần Hưng Đạo Bình Thuận năm 2016 2017 (có lời giải chi tiết)
Đề thi chính thức vào 10 môn Hóa Hệ chuyên THPT Chuyên Trần Hưng Đạo Bình Thuận năm 2016 2017...
Câu 1 :
(2,0 điểm)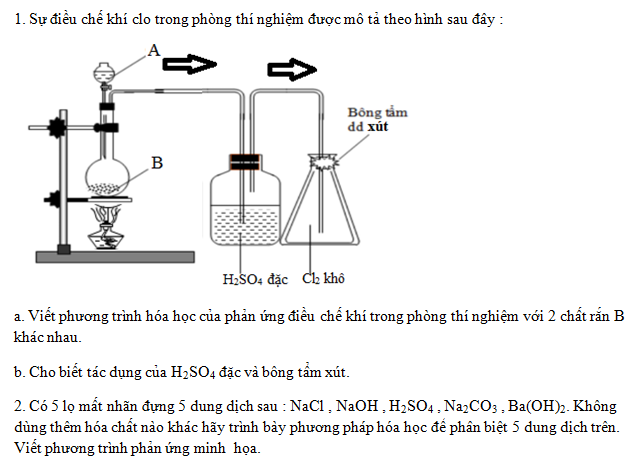
Câu 6 :
(2,0 điểm)
Lời giải có ở chi tiết câu hỏi nhé! (click chuột vào câu hỏi).
Copyright © 2021 HOCTAP247
