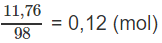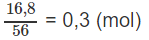Trang chủ
Đề thi & kiểm tra
Lớp 11
Hóa học
Giải SBT Hóa học 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng !!
Rót dung dịch chứa 11,76 g H3PO4 vào dung dịch...
Rót dung dịch chứa 11,76 g H3PO4 vào dung dịch chứa 16,8 g KOH
Câu hỏi :
Rót dung dịch chứa 11,76 g vào dung dịch chứa 16,8 g KOH. Sau phản ứng cho dung dịch bay hơi đến khô. Tính khối lượng muối khan thu được.
* Đáp án
* Hướng dẫn giải
Số mol :
Số mol KOH:
Các phản ứng có thể xảy ra :
Vì tỉ lệ nKOH : = 0,3 : 0,12 = 2,5 nằm giữa 2 và 3, nên chỉ xảy ra các phản ứng (2) và (3), nghĩa là tạo ra hai muối và
Gọi x là số mol tham gia phản ứng (2) và y là số mol tham gia phản ứng (3) :
x + y = 0,12 (a)
Theo các phản ứng (2) và (3) tổng số mol KOH tham gia phản ứng :
2x + 3y = 0,3 (b)
Giải hộ phương trình (a) và (b): x = 0,06 mol ; y = 0,06 mol
Tổng khối lượng hai muối:
mK2HPO4 + mK3PO4 = 0,06 x 174 + 0,06 x 212 = 10,44 + 12,72 = 23,16 (g).
Câu hỏi trên thuộc đề trắc nghiệm dưới đây !
Giải SBT Hóa học 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng !!
Số câu hỏi: 8
Copyright © 2021 HOCTAP247