Trang chủ
Đề thi & kiểm tra
Lớp 9
Hóa học
38 Đề thi chính thức vào 10 môn Hóa cực hay có lời giải chi tiết !!
38 Đề thi chính thức vào 10 môn Hóa cực hay có lời giải chi tiết !!
Câu 16 : Nhỏ chậm nước vào nhôm cacbua
Câu 48 : Cho sơ đồ chuyển hóa sau:
Câu 69 : Chọn phát biếu đúng - sai
Câu 75 : Bốn chất hữu cơ có công thức phân tử là C2H4, C2H6O, C2H4O2, C4H8O2 thực hiện được chuyển hóa sau:
Câu 91 : Hãy chọn các chất thích hợp và viết các phương trình phản ứng hoàn thành sơ đồ chuyển hóa sau:
Câu 102 : Polime X được tạo bởi một loại mắt xích có 38,4% cacbon; 56,8% clo ; còn lại là hiđro về khối lượng.
Câu 147 : Tiến hành thí nghiệm sau:
Câu 183 : Cho dãy chuyển hóa sau:
Câu 192 : Cho sơ đồ chuyển hóa sau:
Câu 199 : Chia hỗn hợp M gồm axit hữu cơ A (CnH2n+1COOH) và rượu B (CmH2m+1OH) làm ba phần bằng nhau:
Câu 211 : Chất bột A là Na2CO3, chất bột B là Ca(HCO3)2. Viết phương trình hóa học xảy ra (nếu có) khi:
Câu 218 : Cho các chất X, Y, Z, T đơn chức, mạch hở có cùng công thức phân tử là C4H6O2 và có đặc điểm sau:
Câu 229 : Xác định A, B, C và viết phương trình hóa học (ghi rõ điều kiện nếu có) cho dãy chuyển đổi sau:
Câu 246 :
Viết phương trình phản ứng theo sơ đồ chuyển hóa sau (mỗi mũi tên là một phương trình phản ứng):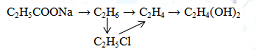
Câu 252 : Hai loại nguyên tử X và Y tạo được với nhau 2 phân tử XY3 và X2Y4. Trong hai phân tử đó thì:
Câu 255 : Trình bày phương pháp hóa học để tách riêng từng chất tinh khiết từ hỗn hợp gồm C2H5OH, CH3COOH
Câu 268 : Giải thích vì sao:
Câu 301 : Tiến hành các thí nghiệm sau:
Câu 312 : Cho sơ đồ chuyển hóa sau:
Câu 325 : Cho sơ đồ sau:
Câu 343 : Chỉ dùng thêm một kim loại để nhận biết 4 dung dịch không màu bị mất nhãn K2SO4, K2SO3, HCl, BaCl2
Câu 346 : Cho hình vẽ sau:
Câu 349 : Cho dãy chuyển hóa sau:
Câu 367 : Cho mẩu Na vào dung dịch FeCl3.
Câu 378 : Đốt cháy hoàn toàn 0,1 mol một este đơn chức, mạch hở X, thu được 17,6 gam CO2 và 7,2 gam H2O.
Lời giải có ở chi tiết câu hỏi nhé! (click chuột vào câu hỏi).
Copyright © 2021 HOCTAP247
