Nhỏ từ từ dung dịch H2SO4 vào 200ml hỗn hợp Ba(OH)2 aM và Ba(AlO2)2 bM, kết quả thí nghiệm thu được như hình v�
Câu hỏi :
Nhỏ từ từ dung dịch H2SO4 vào 200ml dung dịch hỗn hợp Ba(OH)2 aM và Ba(AlO2)2 bM, kết quả thí nghiệm thu được như hình vẽ dưới đây: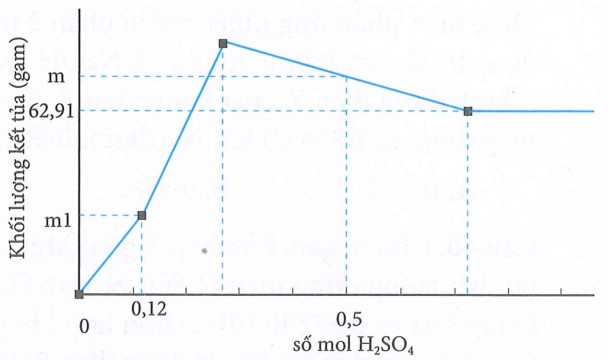
A. 96,07 gam.
B. 102,31 gam.
C. 90,87 gam.
D. 108,81 gam.
* Đáp án
B
* Hướng dẫn giải
Đáp án B
Ta có: \(\left\{ \begin{array}{l} {n_{Ba{{(OH)}_2}}} = 0,2a(mol)\\ {n_{Ba{{(Al{O_2})}_2}}} = 0,2b(mol) \end{array} \right. \to \left\{ \begin{array}{l} {n_{B{a^{2 + }}}} = 0,2(a + b)(mol)\\ {n_{O{H^ - }}} = 0,4a(mol)\\ {n_{AlO_2^ - }} = 0,4b(mol) \end{array} \right.\)
Tại \({{n}_{{{H}_{2}}S{{O}_{4}}}}=0,12mol\to \) trung hòa hết OH- đồng thời tạo kết tủa của BaSO4
Khi đó: \({{n}_{{{H}^{+}}}}={{n}_{O{{H}^{-}}}}\to 0,4a=0,12.2\to a=0,6\to {{m}_{BaS{{O}_{4}}}}=0,12.233=27,96(g)={{m}_{1}}\,\,\,\,(1)\)
+) Tại \({{m}_{\downarrow }}=62,91(g)\to Al{{(OH)}_{3}}\) tan hết kết tủa chỉ còn BaSO4 \)\to {{m}_{BaS{{O}_{4}}}}=62,91(g)\)
\(\to {{n}_{Ba}}S{{O}_{4}}=0,27\,mol\to 0,2(a+b)=0,27\to b=0,75\to {{n}_{AlO_{2}^{-}}}=0,3\,mol\)
+) Tại \({{n}_{{{H}_{2}}S{{O}_{4}}}}=0,5mol\to \left\{ \begin{align} & BaS{{O}_{4}}_{\max } \\ & Al{{(OH)}_{3}} \\ \end{align} \right.\)
Ta có: \({{n}_{Al{{(OH)}_{3}}}}=\frac{4.{{n}_{AlO_{2}^{-}}}-{{n}_{{{H}^{+}}}}}{3}=\frac{4.0,3-(1-0,24)}{3}=\frac{0,44}{3}\to {{m}_{Al{{(OH)}_{3}}}}=11,44(g)\)
\(\to m+{{m}_{1}}=27,96+62,91+11,44=102,31(gam)\)
Câu hỏi trên thuộc đề trắc nghiệm dưới đây !
Đề thi thử THPT QG năm 2022 môn Hóa học Trường THPT Nguyễn Hữu Cảnh
Copyright © 2021 HOCTAP247
