Trang chủ
Đề thi & kiểm tra
Lớp 12
Hóa học
Đề thi thử THPT QG Hóa học 12 - THPT Hàn Thuyên - Bắc Ninh
Đốt cháy 24,48 gam hỗn hợp X gồm glucozơ và...
Đốt cháy 24,48 gam hỗn hợp X gồm glucozơ và saccacrozơ cần dùng 0,84 mol O2.
Câu hỏi :
Đốt cháy 24,48 gam hỗn hợp X gồm glucozơ và saccacrozơ cần dùng 0,84 mol O2. Mặt khác đun nóng 24,48 gam X trong môi trường axit, thu được hỗn hợp Y gồm các hợp chất hữu cơ. Cho toàn bộ Y tác dụng với lượng dư dung dịch AgNO3/NH3 đun nóng, thu được m gam AgCác phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 43,20 gam
B. 25,92 gam
C. 34,56 gam
D. 30,24 gam
* Đáp án
D
* Hướng dẫn giải
Gọi số mol Glucozơ và Saccarozơ lần lượt là x,y mol
C6H12O6 +6O2 → 6CO2 + 6H2O
C12H22O11 + 12O2 → 12CO2 + 11H2O
\(\left\{ \begin{array}{l}
m = 180x + 342y = 24,48\\
{n_{{O_2}}} = 6x + 12 = 0,84
\end{array} \right. \to \left\{ \begin{array}{l}
x = 0,06\\
y = 0,04
\end{array} \right.\)
Khi thủy phân X chỉ có Saccarozơ bị thủy phân:
Saccarozơ →Glucozơ+Fructozơ
0,04 → 0,04 → 0,04
Sau khi thủy phân : nglucozơ = 0,06+ 0,04 = 0,1; nfructozơ = 0,04
Ta có: 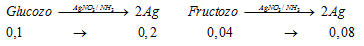
Vậy tổng số mol Ag là: 0,2+0,08=0,28 mol.→ mAg = 0,28.108 = 30,24g
Câu hỏi trên thuộc đề trắc nghiệm dưới đây !
Đề thi thử THPT QG Hóa học 12 - THPT Hàn Thuyên - Bắc Ninh
Số câu hỏi: 38
Copyright © 2021 HOCTAP247
