30 Bài tập Tốc độ phản ứng hóa học có lời giải chi tiết !!
Câu 1 : Khẳng định nào sau đây không đúng ?
A. Nhiệt độ của ngọn lửa axetilen cháy trong oxi cao hơn nhiều so với cháy trong không khí.
B. Nấu thực phẩm trong nồi áp suất nhanh chín hơn so với khi nấu chúng ở áp suất thường.
C. Các chất đốt rắn (như than, củi) có kích thước nhỏ hơn sẽ cháy nhanh hơn.
D. Nấu thực phẩm trên núi cao (áp suất thấp) thực phẩm nhanh chín hơn.
Câu 2 : Trong các cặp phản ứng sau, phản ứng nào có tốc độ lớn nhất ?
A. Fe + dung dịch HCl 0,1M.
B. Fe + dung dịch HCl 0,2M.
C. Fe + dung dịch HCl 0,3M.
D. Fe + dung dịch HCl 0,5M.
Câu 3 : Cho phản ứng hóa học: A(k) + 2B(k) + nhiệt → AB2(k). Tốc độ phản ứng sẽ tăng, nếu
A. tăng áp suất.
B. tăng thể tích của bình phản ứng
C. giảm áp suất.
D. giảm nồng độ khí A
Câu 4 : Tăng diện tích bề mặt của chất phản ứng trong một hệ dị thể, kết quả sẽ là :
A. Giảm tốc độ phản ứng.
B. Tăng tốc độ phản ứng.
C. Giảm nhiệt độ phản ứng.
D. Tăng nhiệt độ phản ứng.
Câu 5 : Cho phản ứng: Zn(r) + 2HCl(dd) → ZnCl2(dd) + H2(k)
A. Giảm, tốc độ phản ứng tạo ra sản phẩm tăng.
B. Giảm, tốc độ phản ứng tạo ra sản phẩm giảm.
C. Tăng, tốc độ phản ứng tạo ra sản phẩm tăng.
D. Tăng, tốc độ phản ứng tạo ra sản phẩm giảm.
Câu 6 : Khi cho cùng một lượng dung dịch axit sunfuric vào hai cốc đựng cùng một thể tích dung dịch Na2S2O3 với nồng độ khác nhau, ở cốc đựng dung dịch Na2S2O3 có nồng độ lớn hơn thấy xuất hiện kết tủa trước. Điều đó chứng tỏ, ở cùng điều kiện nhiệt độ, tốc độ phản ứng:
A. không phụ thuộc nồng độ của chất phản ứng.
B. tỉ lệ thuận với nồng độ của chất phản ứng.
C. tỉ lệ nghịch với nồng độ của chất phản ứng.
D. không thay đổi khi nồng độ chất phản ứng thay đổi.
Câu 7 : Cho kẽm hạt tác dụng với dung dịch H2SO4 4M ở nhiệt độ thường. Tác động nào sau đây không làm tăng vận tốc của phản ứng ?
A. Dùng kẽm bột thay kẽm hạt.
B. Tiến hành ở nhiệt độ 50oC.
C. Dùng H2SO4 5M.
D. Tăng thể tích dung dịch H2SO4 lên gấp đôi.
Câu 8 : Khi cho axit clohiđric tác dụng với Kali pemanganat (rắn) để điều chế khí clo, để khí clo thoát ra nhanh hơn, ta phải:
A. dùng HCl đặc và đun nhẹ hỗn hợp.
B. dùng HCl loãng và đun nhẹ hỗn hợp.
C. dùng HCl loãng.
D. dùng HCl đặc và làm lạnh hỗn hợp.
Câu 9 : Trong quá trình nung vôi, người ta phải đập nhỏ đá vôi ở kích thước vừa phải. Yếu tố nào đã được vận dụng để làm tăng tốc độ phản ứng ?
A. Nồng độ chất tham gia.
B. Nhiệt độ.
C. Diện tích bề mặt chất rắn.
D. Áp suất.
Câu 10 : Khi tăng nhiệt độ, tốc độ phản ứng tăng là do:
A. số phân tử chất tham gia tăng
B. số va chạm có hiệu quả giữa các phân tử chất tham gia tăng lên.
C. tốc độ chuyển động của các phân tử tăng lên.
D. phản ứng thu nhiệt nên có thêm năng lượng để các chất phản ứng với nhau.
Câu 11 : Yếu tố nào dưới đây không ảnh hưởng đến tốc độ phản ứng sau:
A. Nhiệt độ.
B. Chất xúc tác.
C. Áp suất.
D. Kích thước của các tinh thể KClO3.
Câu 12 : Cho 5 gam Al viên vào cốc đựng 50 ml dung dịch HCl 2M ở nhiệt độ thường. Trường hợp nào sau đây, tốc độ phản ứng không thay đổi ?
A. Thay 5 gam Al viên bằng 5 gam Al bột.
B. Thay dung dịch HCl 2M bằng dung dịch HCl 1M.
C. Tăng nhiệt độ lên 50oC.
D. Tăng lượng dung dịch HCl 2M lên gấp đôi.
Câu 13 : Trong quá trình sản xuất gang, xảy ra phản ứng :
A. Tăng nhiệt độ phản ứng.
B. Tăng kích thước quặng Fe2O3.
C. Nén khí CO2 vào lò.
D. Giảm áp suất chung của hệ.
Câu 14 : Kẽm đang phản ứng mạnh với axit clohiđric, nếu cho thêm muối natri axetat vào dung dịch thì thấy phản ứng
A. không thay đổi
B. không xác định được
C. nhanh lên
D. chậm lại
Câu 15 : Hai nhóm học sinh làm thí nghiệm: nghiên cứu tốc độ phản ứng kẽm tan trong dung dịch axit clohiđric:
A. Diện tích tiếp xúc bề mặt bột kẽm lớn hơn.
B. Nhóm 2 dùng axit nhiều hơn
C. Nồng độ kẽm bột lớn hơn.
D. Số mol của axit lớn hơn.
Câu 16 : Có 3 cốc chứa 20ml dung dịch H2O2 cùng nồng độ. Tiến hành 3 thí nghiệm như hình vẽ sau:
A. Thí nghiệm 1
B. Thí nghiệm 2
C. Thí nghiệm 3
D. 3 thí nghiệm như nhau
Câu 17 : Có 3 xilanh kín, nạp vào mỗi xilanh cùng 1 lượng NO2, giữ cho 3 xilanh cùng ở nhiệt độ phòng và di chuyển pittông của 3 xilanh như hình vẽ. Hỏi ở xilanh nào hỗn hợp khí có màu đậm nhất?
A. Xilanh 2
B. Xilanh 1
C. Xilanh 3
D. Cả 3 có màu như nhau
Câu 18 : Cho cân bằng sau:
A. 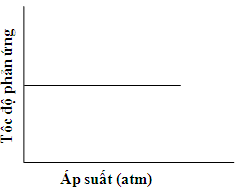
B.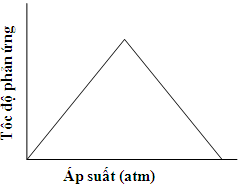
C.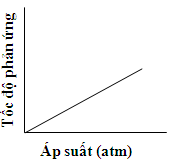
D.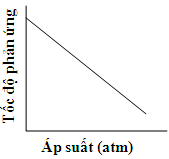
Câu 19 : Tốc độ phản ứng là:
A. Độ biến thiên nồng độ của một chất phản ứng trong một đơn vị thời gian.
B. Độ biến thiên nồng độ của một sản phẩm phản ứng trong một đơn vị thời gian.
C. Độ biến thiên nồng độ của một chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian
D. Độ biến thiên nồng độ của các chất phản ứng trong một đơn vị thời gian.
Câu 20 : Dùng không khí nén thổi vào lò cao để đốt cháy than cốc (trong sản xuất gang), yếu tố nào ảnh hưởng đến tốc độ phản ứng ?
A. Nhiệt độ, áp suất.
B. tăng diện tích.
C. Nồng độ.
D. xúc tác.
Câu 21 : Có phương trình phản ứng: 2A + B → C. Tốc độ phản ứng tại một thời điểm được tính bằng biểu thức v=k[A]2.[B]. Hằng số tốc độ k phụ thuộc:
A. Nồng độ của chất A
B. Nồng độ của chất B
C. Nhiệt độ của phản ứng
D. Thời gian xảy ra phản ứng.
Câu 22 : Khi ninh (hầm) thịt cá, người ta làm gì cho chúng nhanh chín ?
A. Dùng nồi áp suất
B. Chặt nhỏ thịt cá.
C. Cho thêm muối vào.
D. Cả 3 đều đúng
Câu 23 : Tăng nhiệt độ của một hệ phản ứng sẽ dẫn đến sự va chạm có hiệu quả giữa các phân tử chất phản ứng. Tính chất của sự va chạm đó là:
A. Thoạt đầu tăng, sau đó giảm dần.
B. Chỉ có giảm dần.
C. Thoạt đầu giảm, sau đó tăng dần.
D. Chỉ có tăng dần.
Câu 24 : Thực hiện 2 thí nghiệm theo hình vẽ sau. Ở thí nghiệm nào có kết tủa xuất hiện trước?
A. TN1 có kết tủa xuất hiện trước.
B. TN2 có kết tủa xuất hiện trước
C. Kết tủa xuất hiện đồng thời.
D. Không có kết tủa xuất hiện.
Câu 25 : Trong phản ứng tổng hợp amoniac : H2 + 3N2 ⇄ 2NH3. Yếu tố không làm tăng tốc độ phản ứng là
A. tăng nhiệt độ
B. nén hỗn hợp khí nitơ và hiđro trước khi đưa vào tháp tổng hợp
C. thêm chất xúc tác sắt kim loại được trộn thêm Al2O3, K2O...
D. giảm nhiệt độ
Câu 26 : Trong các thí nghiệm sau, nếu lượng Fe trong các cặp đều được lấy bằng nhau thì ở thí nghiệm nào tốc độ phản ứng là lớn nhất ?
A. Fe + dung dịch HCl 0,1M.
B. Fe + dung dịch HCl 0,2M.
C. Fe + dung dịch HCl 0,3M
D. Fe + dung dịch HCl 20% (d = 1,2 g/ml).
Câu 27 : Cho 5 gam kẽm viên vào cốc đựng 50ml dung dịch H2SO4 4M ở nhiệt độ thường (25oC). Có các tác động sau:
A. 3
B. 1
C. 4
D. 2
Câu 28 : Xét phản ứng phân hủy N2O5 trong dung môi CCl4 ở 450C :
A. 1,36.10-3 mol/(l.s).
B. 6,80.10-4 mol/(l.s)
C. 6,80.10-3 mol/(l.s).
D. 2,72.10-3 mol/(l.s).
Lời giải có ở chi tiết câu hỏi nhé! (click chuột vào câu hỏi).
Copyright © 2021 HOCTAP247
