Mô tả sự tạo thành các phân tử sau theo khái niệm lai hóa orbital. a) Phân tử BeH2. b) Phân tử SO2. c) Phân tử NH3.
Câu hỏi :
Mô tả sự tạo thành các phân tử sau theo khái niệm lai hóa orbital.
a) Phân tử BeH2.
b) Phân tử SO2.
c) Phân tử NH3.
Mô tả sự tạo thành các phân tử sau theo khái niệm lai hóa orbital.
a) Phân tử BeH2.
b) Phân tử SO2.
c) Phân tử NH3.
* Đáp án
* Hướng dẫn giải
Trả lời:
a) Phân tử BeH2.
Cấu hình electron hóa trị của Be: 2s2.
Trong nguyên tử Be, một AO 2s tổ hợp với 1 AO 2p, tạo ra hai AO lai hóa sp.
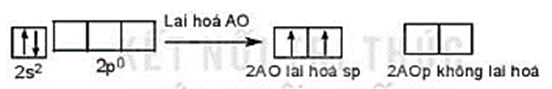
Hai AO lai hóa sp của nguyên tử Be xen phủ với hai AO s của hai nguyên tử H tạo thành hai liên kết σ giữa Be – H.
b) Phân tử SO2.
Cấu hình electron hóa trị của S: 3s23p4.
Trong nguyên tử S, một AO 3s lai hóa với hai AO p, tạo ra ba AO lai hóa sp2.
S còn AO p chứa 1 electron độc thân sẽ xen phủ 1 AO p chứa 1 electron độc thân của O hình thành liên kết π và AO chưa lai hóa có 1 electron độc thân sẽ tiếp tục xen phủ với OA p của nguyên tử O đó để hình thành liên kết σ. Với nguyên tử O còn lại thì nguyên tử S dùng AO chứa 2 electron để xen phủ với 2 AO chứa electron độc thân của nguyên tử O còn lại.
c) Phân tử NH3.
Cấu hình electron hóa trị của N: 2s22p3.
Trong nguyên tử N, 1 AO 2s và 3 AO 2p của nguyên tử N lai hóa với nhau tạo nên 4 AO lai hóa sp3 giống hệt nhau, hướng về 4 đỉnh của hình tứ diện đều. Trên 3 AO lai hóa có electron độc thân. Trên AO lai hóa còn lại có cặp electron ghép đôi.
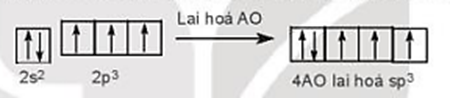
Ba AO lai hóa chứa electron độc thân của nguyên tử N xen phủ với 3 AO 1s chứa electron độc thân của 3 nguyên tử H, tạo nên 3 liên kết σ.
Câu hỏi trên thuộc đề trắc nghiệm dưới đây !
Bài tập Liên kết hóa học có đáp án !!
Copyright © 2021 HOCTAP247
