Phân tử chứa nguyên tử lai hóa sp3 có cấu trúc phẳng không? Giải thích
Câu hỏi :
Phân tử chứa nguyên tử lai hóa sp3 có cấu trúc phẳng không? Giải thích và cho ví dụ.
Phân tử chứa nguyên tử lai hóa sp3 có cấu trúc phẳng không? Giải thích và cho ví dụ.
* Đáp án
* Hướng dẫn giải
Phân tử chứa nguyên tử lai hóa sp3 không thể có cấu trúc phẳng. Vì khi 1 AO ns tổ hợp với 3 AO np tạo ra 4 AO lai hóa sp3. 4 AO sp3 này chiếm 4 khu vực điện tích âm sao cho lực đẩy giữa chúng là nhỏ nhất nên phân tử có dạng tứ diện, góc tạo bởi hai trục của hai AO là 109,5o.
Ví dụ phân tử CH4
Từ công thức Lewis của CH4 ta xác định được phân tử này có dạng tứ diện theo mô hình VSEPR.
Cấu hình electron của C (Z = 6) là 1s22s22p2
1 AO 2s tổ hợp với 3 AO 2p tạo 4 AO lai hóa sp3
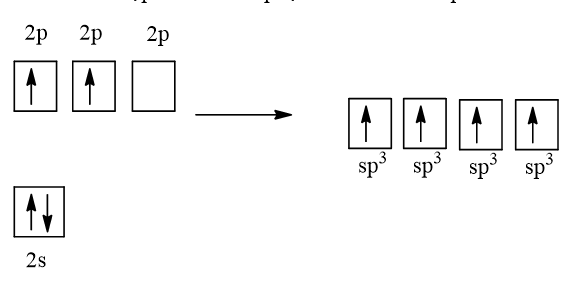
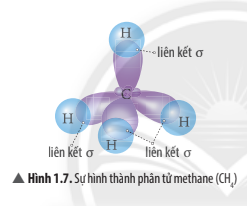
4 AO lai hóa sp3 của nguyên tử C xen phủ với 4 AO s của nguyên tử H tạo thành 4 liên kết σ hướng về 4 đỉnh của một tứ diện đều.
Câu hỏi trên thuộc đề trắc nghiệm dưới đây !
Chuyên đề Hóa 10 Bài 1: Liên kết hóa học có đáp án !!
Copyright © 2021 HOCTAP247
