(2,5 điểm).Cho 3,84 gam hỗn hợp A gồm Mg và FeO tác dụng với dung dịch HCl 0,25M thu được 2,24 lit khí ở đktc.a, Tính phần trăm khối lượng mỗi chất trong hỗn hợp A.b, Tính thể tích...
Câu hỏi :
(2,5 điểm).
* Đáp án
* Hướng dẫn giải
Hướng dẫn giải
a, Phương trình phản ứng:
Mg + 2HCl → MgCl2+ H2
FeO + 2HCl → FeCl2+ H2O
Số mol khí H2thu được là: 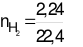 = 0,1 mol
= 0,1 mol
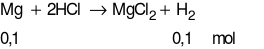
Theo phương trình phản ứng ta có: nMg= 0,1 mol suy mMg= 0,1.24 = 2,4 gam.
Vậy %mMg= 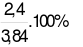 = 62,5%
= 62,5%
%mFeO= 100% - 62,5% = 37,5%
b, Khối lượng của FeO là: mFeO= 3,84 – 2,4 = 1,44 gam
⇒ nFeO= 0,02 mol
Phương trình phản ứng:
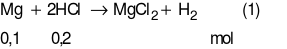
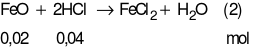
Từ phương trình phản ứng (1) và (2) suy ra nHCl= 0,2 + 0,04 = 0,24 mol
Vậy thể tích dung dịch axit HCl đã dùng là: VHCl= 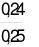 = 0,96 lít
= 0,96 lít
c,
Tỉ khối của Y so với H2bằng 26 suy ra 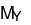 = 52, ta có:
= 52, ta có:
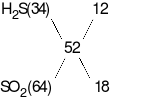
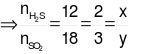
Mặt khác, bảo toàn mol electron ta có: 8x + 2y = 2nMg + nFeO= 0,22
Suy ra x = 0,02 mol; y = 0,03 mol
Vậy V = 22,4.(0,02+0,03) = 1,12 lit
(Họcsinhkhôngđượcsửdụngbảnghệthốngtuầnhoàncácnguyêntốhóahọc)
Câu hỏi trên thuộc đề trắc nghiệm dưới đây !
Đề thi Học kì 2 Hóa học 10 cực hay có đáp án !!
Copyright © 2021 HOCTAP247
